隨著2025年的落幕,中國保健食品行業(yè)的監(jiān)管與發(fā)展脈絡(luò)在這一年的注冊與技術(shù)轉(zhuǎn)讓數(shù)據(jù)中得以清晰呈現(xiàn)。這一年,行業(yè)在規(guī)范化、科學(xué)化與創(chuàng)新化的軌道上持續(xù)深化,政策引導(dǎo)與市場驅(qū)動(dòng)共同塑造了新的產(chǎn)業(yè)格局。本文將對2025年度保健食品的注冊審批情況與技術(shù)轉(zhuǎn)讓市場進(jìn)行系統(tǒng)性盤點(diǎn)與分析。
一、 2025年保健食品注冊審批概況:穩(wěn)中有進(jìn),結(jié)構(gòu)優(yōu)化
- 整體數(shù)據(jù)穩(wěn)中有升:根據(jù)國家市場監(jiān)督管理總局(SAMR)及國家藥品監(jiān)督管理局(NMPA)公開數(shù)據(jù)顯示,2025年全年獲批的保健食品注冊證書數(shù)量較2024年呈現(xiàn)溫和增長態(tài)勢。這表明在歷經(jīng)前幾年的法規(guī)調(diào)整與適應(yīng)期后,企業(yè)申報(bào)的合規(guī)性與成熟度有所提升,審評審批流程的效率也趨于穩(wěn)定。
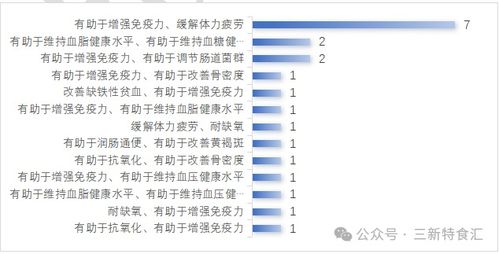
- 功能聲稱分布集中:從獲批產(chǎn)品的功能聲稱來看,增強(qiáng)免疫力、輔助降血脂、緩解體力疲勞、改善睡眠等傳統(tǒng)主流功能依然占據(jù)主導(dǎo)地位。值得注意的是,“輔助改善記憶”、“抗氧化”及針對特定人群(如中老年骨健康、眼部健康)的功能產(chǎn)品的申報(bào)與獲批比例有顯著提升,反映了消費(fèi)者健康需求日益精準(zhǔn)化和細(xì)分化的趨勢。
- 原料創(chuàng)新與安全性并重:新食品原料、特色傳統(tǒng)中藥材(需符合保健食品可用原料目錄)在配方中的應(yīng)用更為活躍。審評環(huán)節(jié)對原料的安全性評估、功效成分的科學(xué)依據(jù)及劑量合理性提出了更高要求。使用新原料的產(chǎn)品其審評周期相對較長,體現(xiàn)了監(jiān)管部門對創(chuàng)新與風(fēng)險(xiǎn)控制的平衡。
- “雙軌制”運(yùn)行成熟:備案制與注冊制并行。營養(yǎng)素補(bǔ)充劑類產(chǎn)品通過備案快速上市,已成為市場供給的重要組成部分。而具有特定功能聲稱的注冊制產(chǎn)品,則繼續(xù)扮演著技術(shù)壁壘高、附加值高的角色,是企業(yè)核心競爭力的體現(xiàn)。
二、 技術(shù)轉(zhuǎn)讓市場動(dòng)態(tài):活躍度提升,成為資源配置關(guān)鍵環(huán)節(jié)
技術(shù)轉(zhuǎn)讓是保健食品行業(yè)盤活存量批文、優(yōu)化資源配置、加速產(chǎn)品商業(yè)化的重要途徑。2025年,該市場呈現(xiàn)以下特點(diǎn):
- 交易活躍,價(jià)值凸顯:受部分企業(yè)戰(zhàn)略聚焦、業(yè)務(wù)調(diào)整或資金回籠需求影響,以及新進(jìn)入者尋求快速獲得市場準(zhǔn)入資格的需求驅(qū)動(dòng),保健食品注冊證書的技術(shù)轉(zhuǎn)讓交易數(shù)量與金額均保持活躍。一些歷史悠久、功能聲稱經(jīng)典、市場認(rèn)知度高的“藍(lán)帽子”批文,尤其受到青睞。
- 轉(zhuǎn)讓標(biāo)的更趨規(guī)范:買賣雙方對轉(zhuǎn)讓標(biāo)的的合規(guī)性審查空前嚴(yán)格。重點(diǎn)關(guān)注方面包括:批文歷史沿革是否清晰、注冊資料與原始檔案是否完整、配方原料是否符合現(xiàn)行法規(guī)標(biāo)準(zhǔn)、生產(chǎn)資質(zhì)(是否具備相應(yīng)劑型的GMP條件)是否匹配、是否存在知識產(chǎn)權(quán)糾紛或未決訴訟等。盡職調(diào)查成為交易達(dá)成的必要前置程序。
- 轉(zhuǎn)讓模式多元化:
- 直接所有權(quán)轉(zhuǎn)讓:最為傳統(tǒng)和徹底的方式。
- 合作開發(fā)與銷售授權(quán):批文持有方以授權(quán)生產(chǎn)、銷售分成等形式與具備市場渠道或生產(chǎn)能力的方合作,降低了直接轉(zhuǎn)讓的風(fēng)險(xiǎn),實(shí)現(xiàn)了優(yōu)勢互補(bǔ)。
- 技術(shù)入股:以批文評估作價(jià),入股新公司,共享長期發(fā)展收益。
- 價(jià)格影響因素復(fù)雜化:批文轉(zhuǎn)讓價(jià)格不僅取決于功能聲稱的熱門程度,更與其科學(xué)依據(jù)的扎實(shí)程度、臨床試驗(yàn)數(shù)據(jù)的完備性、市場容量、品牌潛力、剩余有效期以及轉(zhuǎn)讓后變更(如企業(yè)名稱、地址變更,乃至配方微調(diào))的難易度和成本密切相關(guān)。稀缺的、有扎實(shí)科學(xué)背書的優(yōu)質(zhì)批文價(jià)值持續(xù)走高。
三、 面臨的挑戰(zhàn)與監(jiān)管重點(diǎn)
- 科學(xué)評價(jià)要求持續(xù)提高:監(jiān)管部門對功效聲稱的證據(jù)等級要求不斷提升,尤其是對于創(chuàng)新功能和新原料,需要提供更嚴(yán)謹(jǐn)?shù)娜梭w試驗(yàn)數(shù)據(jù)或系統(tǒng)性的科學(xué)文獻(xiàn)依據(jù)。
- 全生命周期監(jiān)管強(qiáng)化:從注冊審評到上市后監(jiān)督,包括生產(chǎn)合規(guī)性、廣告宣傳真實(shí)性、不良反應(yīng)監(jiān)測等環(huán)節(jié)的監(jiān)管鏈條愈發(fā)緊密。技術(shù)轉(zhuǎn)讓后的產(chǎn)品,其質(zhì)量責(zé)任主體同步轉(zhuǎn)移,受讓方需承擔(dān)起全生命周期的管理責(zé)任。
- 技術(shù)轉(zhuǎn)讓過程中的合規(guī)風(fēng)險(xiǎn):如何確保轉(zhuǎn)讓過程符合《保健食品注冊與備案管理辦法》及相關(guān)規(guī)定,順利完成注冊人/持有人的變更程序,避免出現(xiàn)“影子工廠”、質(zhì)量體系脫節(jié)等問題,是買賣雙方共同面臨的實(shí)操挑戰(zhàn)。
四、 未來展望與建議
保健食品行業(yè)的注冊與技術(shù)轉(zhuǎn)讓將呈現(xiàn)以下趨勢:
- 注冊端:將更加側(cè)重于精準(zhǔn)營養(yǎng)、個(gè)性化健康解決方案方向的產(chǎn)品開發(fā)。基于基因組學(xué)、代謝組學(xué)等現(xiàn)代生物技術(shù)的功能研究可能為注冊提供新路徑。審評審批的數(shù)字化、智能化水平有望進(jìn)一步提升。
- 技術(shù)轉(zhuǎn)讓端:市場將更加專業(yè)化、透明化,可能出現(xiàn)更多提供批文價(jià)值評估、法律盡調(diào)、交易撮合服務(wù)的第三方專業(yè)機(jī)構(gòu)。合規(guī)、高效、安全的轉(zhuǎn)讓流程將成為行業(yè)標(biāo)配。
給行業(yè)參與者的建議:
1. 對于研發(fā)與注冊方:應(yīng)深耕具有堅(jiān)實(shí)科學(xué)基礎(chǔ)的功能研究,注重知識產(chǎn)權(quán)的全局布局,提升注冊資料的質(zhì)量。
2. 對于技術(shù)轉(zhuǎn)讓方/受讓方:務(wù)必重視全面的盡職調(diào)查,借助專業(yè)法律與注冊顧問的力量,確保交易合法合規(guī),實(shí)現(xiàn)批文價(jià)值的平穩(wěn)、有效轉(zhuǎn)移與增值。
3. 對于生產(chǎn)企業(yè):無論通過自研注冊還是受讓獲得批文,都必須嚴(yán)格落實(shí)主體責(zé)任,確保從原料到銷售的全過程質(zhì)量安全管理體系有效運(yùn)行。
2025年的盤點(diǎn)顯示,中國保健食品行業(yè)正穿越周期,走向一個(gè)更加注重科學(xué)、合規(guī)與價(jià)值創(chuàng)造的新階段。注冊證書作為核心的市場準(zhǔn)入資產(chǎn),其創(chuàng)造與流轉(zhuǎn)的每一個(gè)環(huán)節(jié),都深刻影響著行業(yè)的健康與可持續(xù)發(fā)展。